中文标题:Circ-FBXW7在抑制胶质瘤发生中的新作用
发表期刊:JNCI J Natl Cancer Inst
中科院分区:1区
影响因子:11.816
发表时间:2018年3月
合作单位:中山大学第一附属医院
运用技术:LC-MS/MS蛋白质谱鉴定(由辉骏生物提供技术支持,点击查看详情)
● 研究背景
环状RNA(CircRNA)是广泛存在于真核生物基因组中的RNA转录本。据报道,CircRNA在组织发育、基因调控和癌症发生中都起着重要作用,是近来的一大研究热点。然而,对于CircRNA是否编码功能蛋白还有待进一步探究。
● 研究结果
1. CircRNA在人脑胶质母细胞瘤及癌旁正常组织中的不同表达模式
为了建立CircRNA图谱数据库,研究者对来自临床胶质母细胞瘤组织及其配对的正常组织的核糖体RNA缺失的总RNA进行了RNA-seq分析,共鉴定出31145个CircRNA(图1A),使用RefSeq数据库进行注释,这些CircRNA大多来自蛋白质编码的外显子,其他的与内含子、5’-UTR、3’-UTR或反义序列比对(图1B)。这些已鉴定的CircRNA大多数小于1500个核苷酸(图1C),且在癌组和正常组的染色体分布无明显差异,而癌组中的CircRNA总表达下调(图1D,E)。癌组和肿瘤组具有不同的CircRNA表达模式(图1F)。研究者将癌症组和正常组之间差异最大的候选基因与circRNADb进行匹配,在这些特定的候选基因中,由FBXW7基因外显子3和外显子4环化而成的新基因Circ_022705引起了研究者的注意(图2A)。
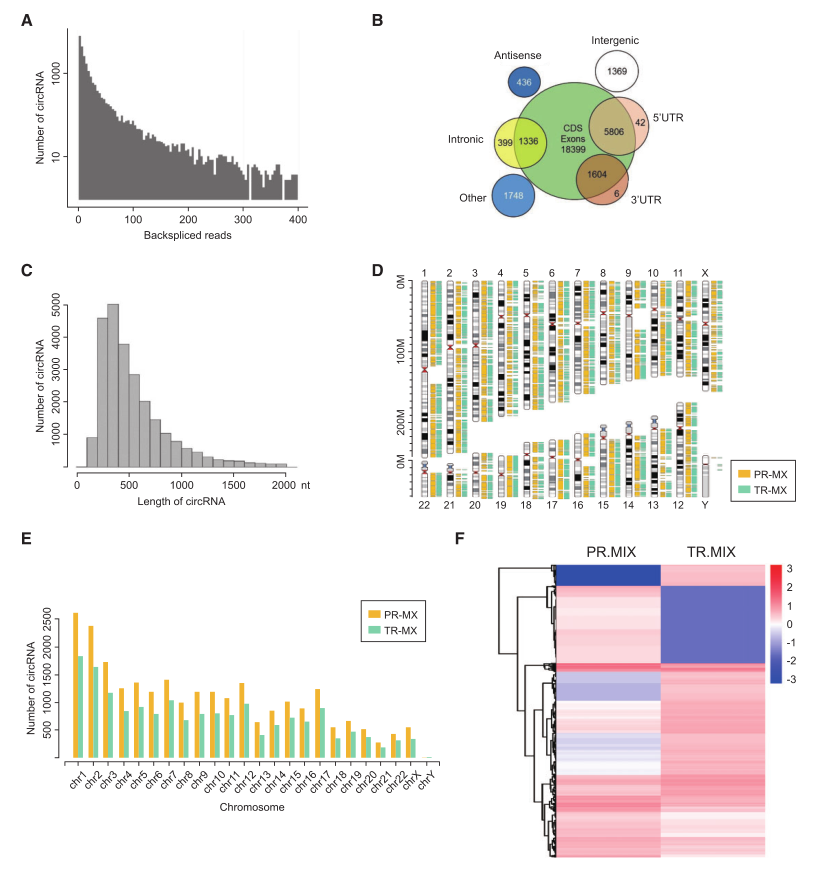
图1
2. 环状RNA Circ-FBXW7的鉴定
为了验证FBXW7基因的外显子3和4是否形成了内源性CircRNA,研究者设计了聚合和发散引物,专门扩增FBXW7的规范形式或后剪接形式(图2B)。Circ-FBXW7基因不能被RNase-R酶切,这些不同的引物不能在基因组DNA中扩增出任何产物,表明这一结果不是由于PCR产物或基因组重排造成的。研究者用跨越结引物验证了RNA-Seq数据,qPCR检测了100例胶质瘤标本和100例正常脑组织中Circ-FBXW7的表达。在胶质瘤中,FBXW7的表达低于正常脑组织(图2C)。桑格测序发现,反向剪接形成了620nt的Circ-FBXW7,推测可能是由于内含子序列的剪切所致。在Northern blotting中,使用连接特异性探针进一步检测到内源CircFBXW7(图2E)。为了证明Circ-FBXW7的细胞定位,研究者进行了FISH分析,结果显示胞浆中有丰富的Circ-FBXW7表达。当转染SiRNA时,Circ-FBXW7的表达被抑制(图2F)。对不同细胞组分的qPCR分析也进一步证实,Circ-FBXW7主要定位于细胞质中(图2F)。
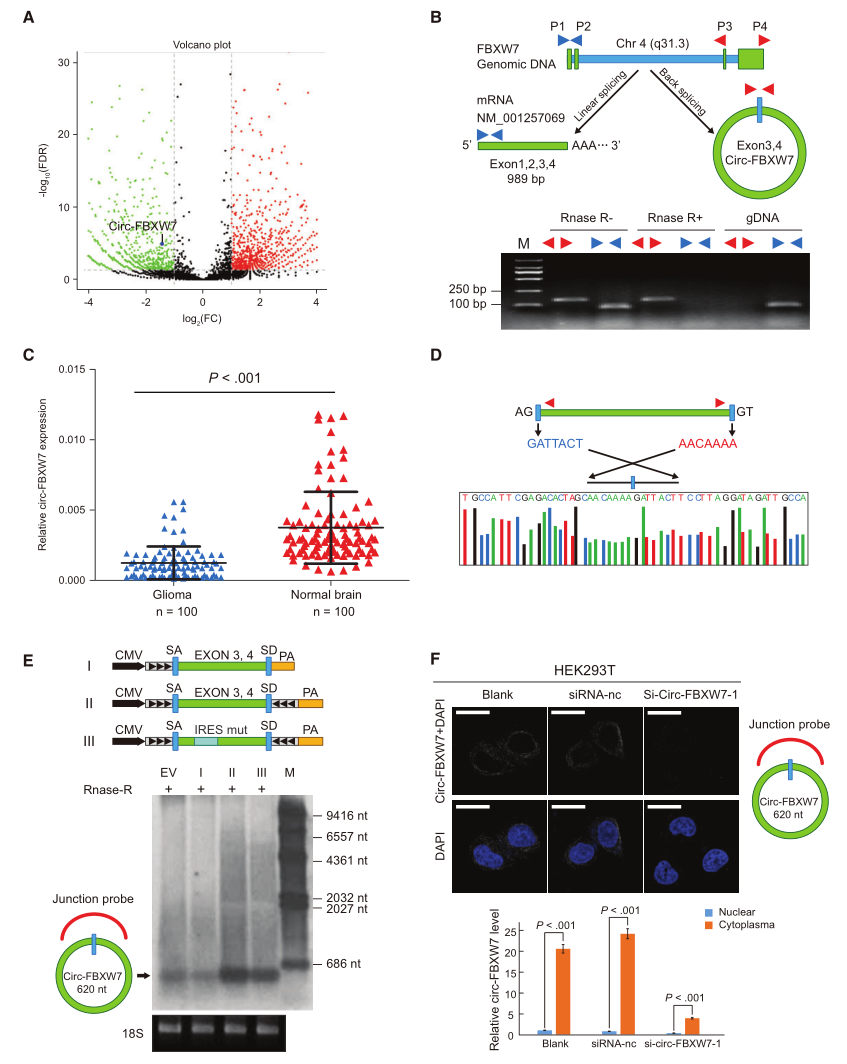
图2
3. Circ-FBXW7编码能力的评估
研究者分析了Circ-FBXW7的开放阅读框(ORF),发现在Circ-FBXW7中有一个潜在的跨越连接ORF,编码185个氨基酸的蛋白质(图3A)。为了测试Circ-FBXW7中可能的IRES活性,研究者使用双酶载体系统在Rluc和Luc报告基因之间克隆了全长或截短的FBXW7 IRES序列。荧光素酶分析表明,与截短或突变的IRES相比,全长Circ-FBXW7 IRES诱导的LUC/Rluc活性最高,相反,空载体不能诱导LUC激活(图3B)。这些结果表明,Circ-FBXW7 IRES可以诱导50个上限的独立翻译。接下来,研究者建立了一组载体来证实Circ-FBXW7在人类细胞中是可翻译的。结果显示,FLAG标签抗体在Circ-FBXW7-FLAG和FBXW7-FLAG转基因细胞中仅检测到约22 kDa的蛋白,表明Circ-FBXW7-FLAG载体已被翻译(图3C)。接下来,研究者用液相色谱串联质谱在Circ-FBXW7-293T细胞中分析了FBXW7-185aa的氨基酸序列。由于FBXW7185aa是由“跨越连接ORF”形成的,在该区域发现的独特氨基酸进一步表明这个新的蛋白质是由Circ-FBXW7编码的(图3C,D)。
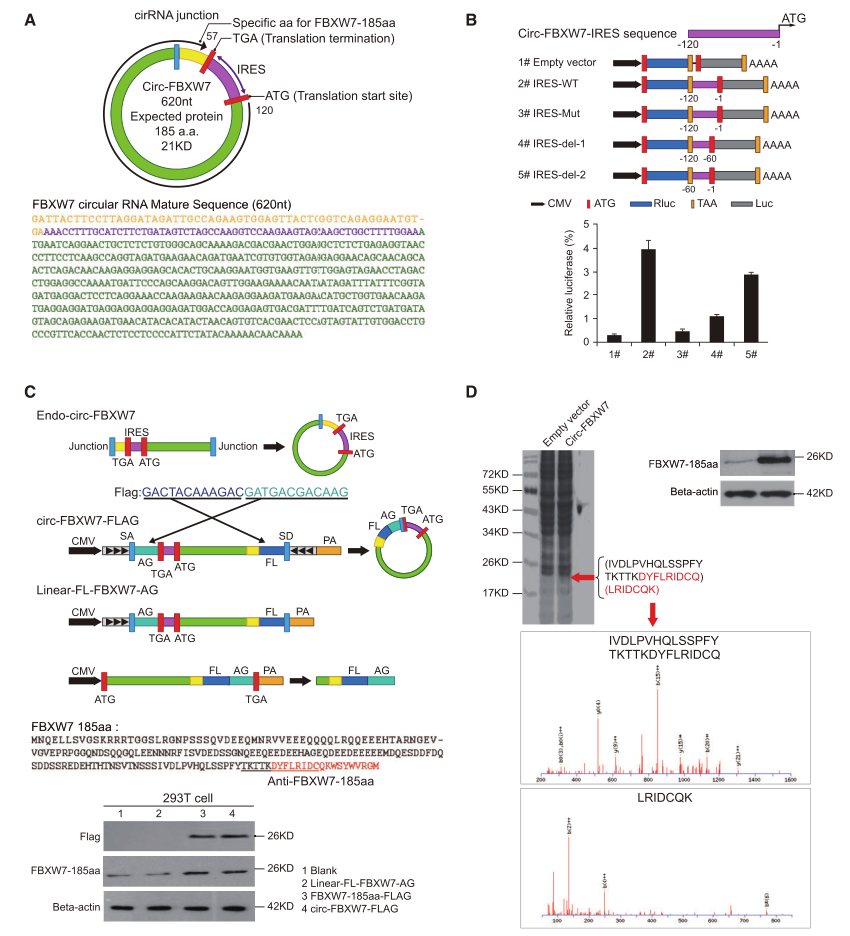
图3
4. FBXW7-185aa对胶质瘤细胞的作用及其分子机制
为了排除Circ-FBXW7而不是FBXW7-185aa诱导生物学功能的可能性,研究者使用图3C中描述的线性FBXW7-FLAG载体建立了稳定高表达U251和U373的FBXW7-185aa细胞。通过使用Circ-FBXW7连接引物,我们发现Circ-FBXW7和Circ-FBXW7-IRES两个mut载体都成功地过表达(图4A)。此外,只有Circ-FBXW7和FBXW7-FLAG载体的过表达才能上调FBXW7-185aa的表达(图4B)。接下来,研究者检测了这些细胞的细胞周期和细胞增殖率。Circ-FBXW7和FBXW7-FLAG稳定过表达的U251和U373细胞与对照细胞相比,表现出大量的G1期阻滞(图4C),存活率也大大降低降低(图4D,E)。用特异性shRNA敲除Circ-FBXW7可降低FBXW7-185aa的表达(图4F),并加速细胞周期,提高细胞存活率(图4G-I)。这些结果表明,FBXW7-185aa(而不是Circ-FBXW7)能够诱导胶质瘤细胞周期停滞,抑制细胞增殖。
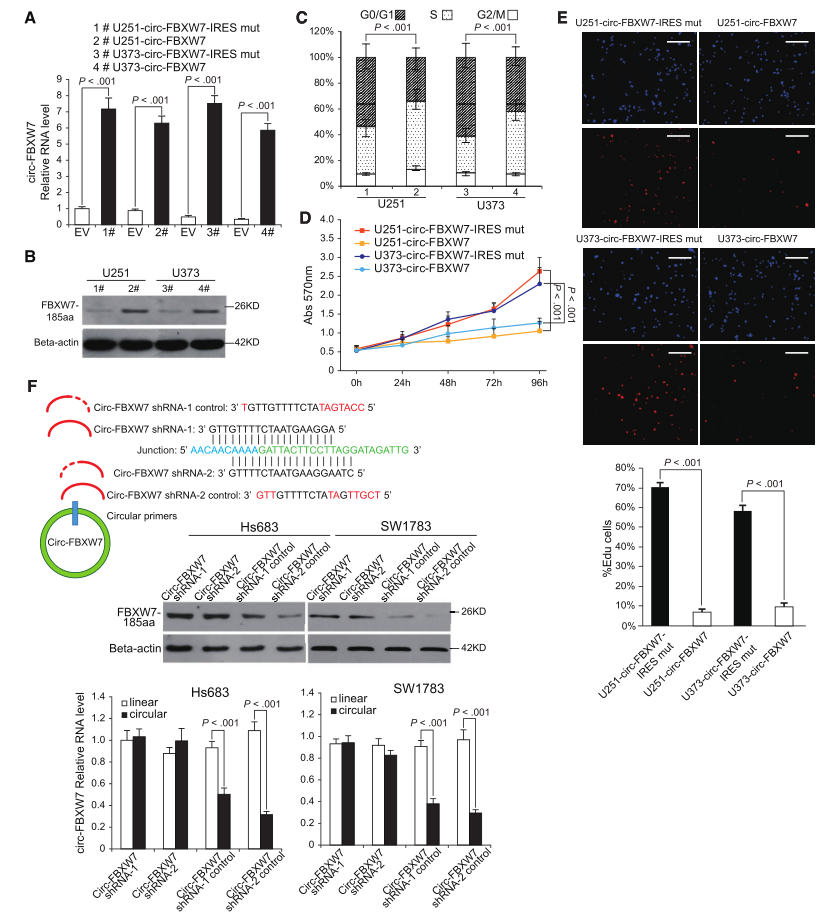
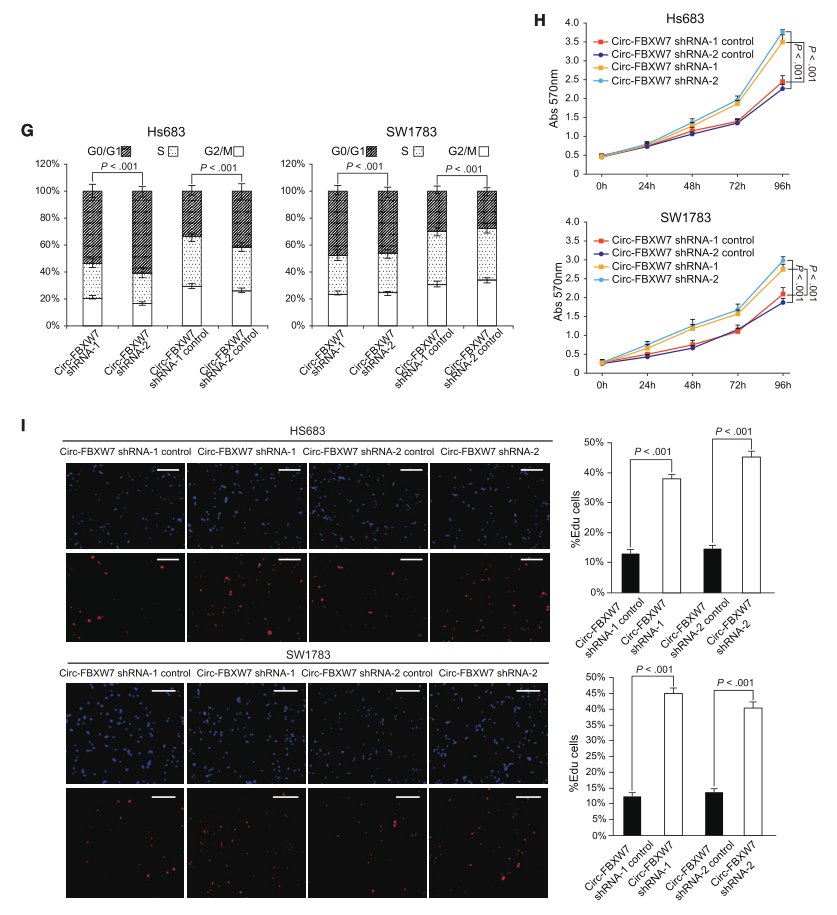
图4
FBXW7α是FBXW7基因中含量最丰富的亚型,是一种定义明确的E3连接酶,可以针对c-Myc进行泛素化诱导的降解。研究者发现在Circ-FBXW7-和FBXW7-185aa过表达的细胞中c-Myc的表达都降低(图5A)。鉴于上述证据,研究者推测FBXW7-185aa可能也有助于c-Myc蛋白的稳定。半衰期试验证实,与阴性对照相比,FBXW7-185aa对c-Myc具有去稳定化作用。此外,FBXW7-185aa比FBXW7α更稳定(图5B)。据报道,去泛素化酶USP28通过与FBXW7αN端的相互作用与c-Myc结合,从而稳定c-Myc。研究者推测FBXW7185aa可能通过USP28破坏c-Myc的稳定性,Pull-down实验和CoIP实验表明,FBXW7-185aa在体外和体内与USP28相互作用(图5C,D)。与FBXW7α相比,FBXW7-185aa与USP28具有更高的结合亲和力,增加FBXW7-185aa可以竞争性地将FBXW7α从癌细胞中的USP28中释放出来(图5E)。体内和体外泛素化实验表明,FBXW7185aa过表达可拮抗USP28诱导的c-Myc去泛素化,增加c-Myc泛素化。然而,仅凭FBXW7-185aa并不能泛化c-Myc(图5F)。在Hs683和SW1783细胞中,FBXW7-185aa的过表达不能抑制c-Myc的表达,表明FBXW7-185aa通过FBXW7a调节c-Myc。此外,过表达USP28抑制了FBXW7-185aa诱导的c-Myc翻转(图5G)。以上证据共同阐明了FBXW7-185aa与USP28竞争性相互作用并“释放”FBXW7α降解c-Myc。
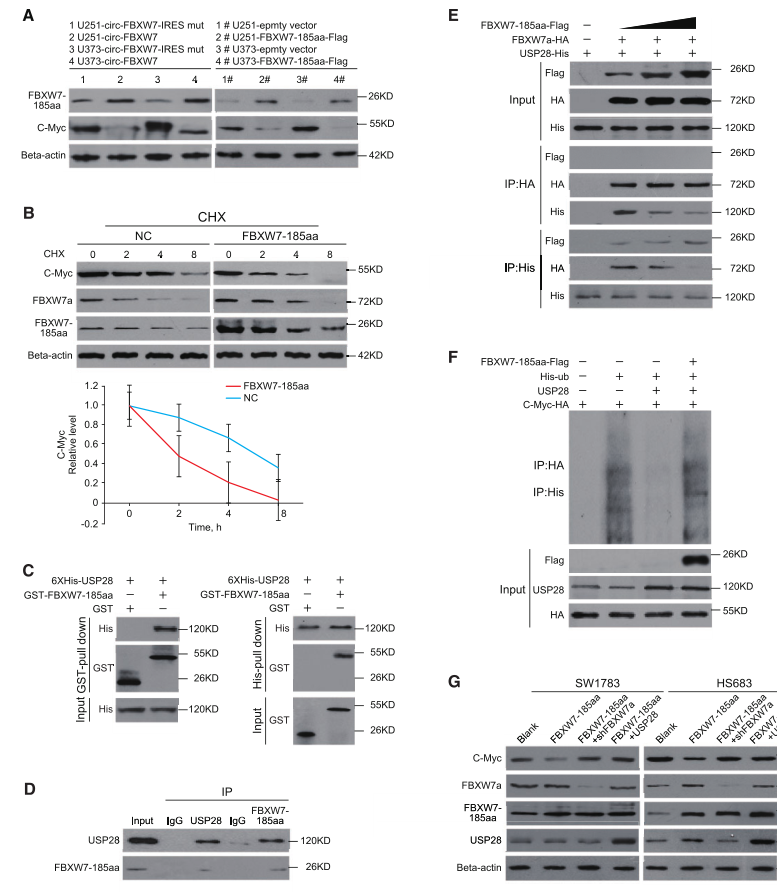
图5
5. Circ-FBXW7和FBXW-185aa的临床意义
为了探索FBXW7-185aa潜在的临床意义,研究者检测了FBXW7-185aa在几个已建立的胶质瘤细胞系中的表达。NHA和293T细胞FBXW7-185aa表达较强;SW1783和Hs683Ⅲ级胶质瘤细胞中FBXW7-185aa表达降低;胶质母细胞瘤细胞系U251和U373中FBXW7-185aa的表达水平最低。与肿瘤旁组织相比,在随机选择的6个胶质母细胞瘤患者样本中FBXW7-185aa和Circ-FBXW7的表达相对降低(图6A)。接下来,研究者检测了38对来源于胶质母细胞瘤患者的癌组织和癌旁组织中Circ-FBXW7的表达,结果显示在胶质母细胞瘤组织中,FBXW7的表达低于癌旁组织,同时Circ-FBXW7高表达的胶质母细胞瘤患者比低表达Circ-FBXW7的患者总生存期更长(图6B)。由于常见的FBXW7α突变不影响Circ-FBXW7或FBXW7-185aa,研究者推测Circ-FBXW7和FBXW7-185aa是胶质母细胞瘤的独立预后标记物。Circ-FBXW7稳定过表达的U251和U373细胞显示出比对照细胞低得多的致瘤性(图6C),此外,稳定过表达U251和U373细胞的Circ-FBXW7小鼠比对照组的寿命更长(图6D)。
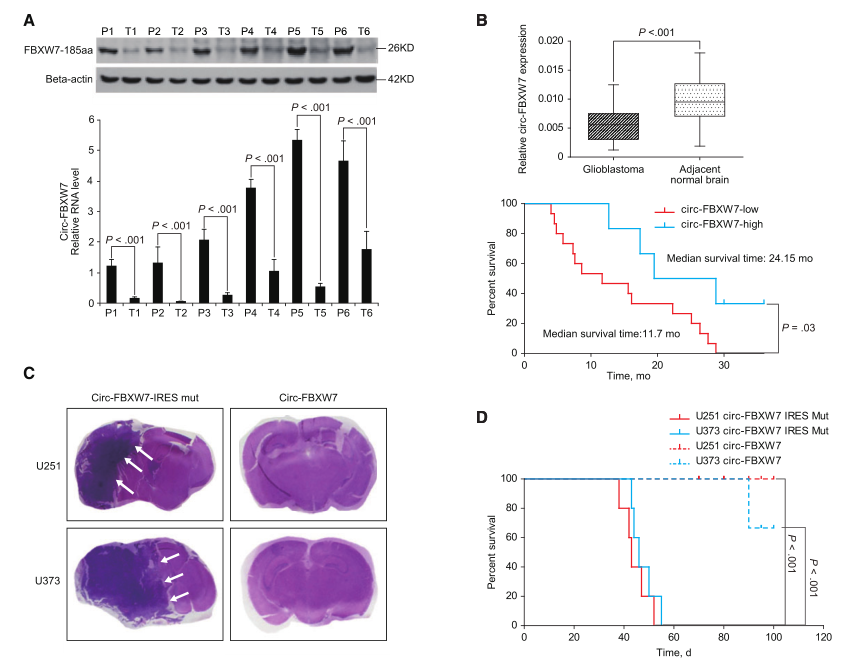
图6









 实验热线:4006991663
实验热线:4006991663











